مقارنة بين قوى التشتت وقوى ثنائية القطب، كل هذه المواد في هذا الكون الواسع، بمختلف أنواعها وحالاتها، تتكون من ثلاثة أشكال، وهي العناصر والمخاليط والمركبات، وكل هذه الأشكال تتكون من جسيمات، وهذه الجسيمات هي جزيئات وذرات وأيونات، المواد قوية جدًا بالنسبة لنا للحصول على مواد صلبة وأقل ضعفًا للحصول على سوائل ثم مواد غازية، وأشهر قوى الجذب هي قوى التشتت والقوى ثنائية القطب، دعنا نقارن بينها.
قوى التشتيت
تُعرف باسم قوى لندن المشتتة أو قوى تشتت فان دير فال ، وهي مرتبطة بين الجسيمات غير القطبية مع بعضها البعض ، وهي جزء من القوى الجذابة التي تسمى قوى فان دير فالس ، والتي أطلق عليها الفيزيائي الألماني الأمريكي فريتز لندن.
إنها قوى جذب بين الجزيئات ، لكنها ضعيفة وتنشأ من الكم الناتج عن الاستقطاب الفوري متعدد الأقطاب بين جزيئات المادة ، وبالتالي فإن قوى تشتت لندن بين الجزيئات تعمل بشكل مؤقت متعدد الأقطاب ، أي مؤقتًا ، وقوى لندن المشتتة يتم عرضها بواسطة الجسيمات غير القطبية بسبب حركات الجسيمات. ربط الإلكترونات في تفاعل الجزيئات.
وقد بدأت عندما اكتشف العلماء أن الغازات النادرة مثل غاز الهيليوم هي ذرات غير مترابطة ، وجزيئات غير قطبية أو محايدة كهربائيًا ، مثل الجزيئات التالية (O2 ، N2 ، C2H4 ، CCl4 ، C6H6) ، يمكن تحويل هذه الجزيئات من الحالة الغازية إلى الحالة السائلة إذا خفضنا درجة حرارتها.
وهذا دليل على أن هناك قوى جاذبة تحدث بينهما حتى تتحول من الحالة الغازية إلى الحالة السائلة التي تكون فيها قوى التجاذب بين الجزيئات والذرات أقوى ، وقد أطلق على هذا الجذب اسم قوى لندن على اسم الفيزيائي الألماني (فريتز لندن) ، لأنه هو الشخص الذي يُنسب إليه الفضل في شرح هذا النوع من الجاذبية في عام 1928.
قوى القطبين
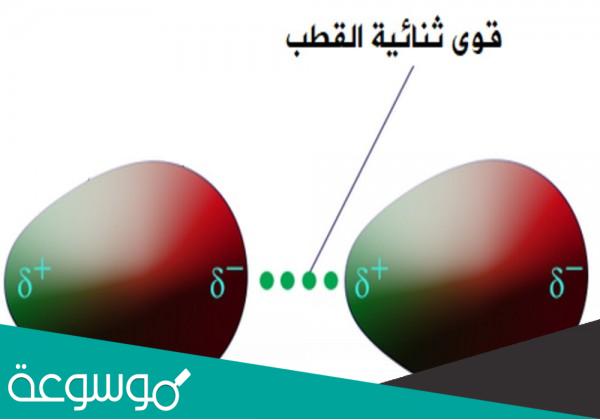
تنشأ هذه القوى بين الجزيئات القطبية ، مثل كلوريد الهيدروجين (HCl) ، وكلوريد اليود (ICl) ، والكلوروفورم (CH3Cl) ، وثاني كلورو ميثان (CH2Cl2). وتتخذ النهايات المختلفة في كل قطب مواضع معاكسة ، مما يجعلها تستجيب وتتحد ، حيث أن أهم العوامل التي تؤثر على القوى الجاذبة في الجزيئات ثنائية القطب هي الطريقة التي يتم بها توجيه هذه الأقطاب.
تميل الجزيئات التي تحتوي على أقطاب سالبة وموجبة إلى ترتيب نفسها ، لذلك يتم توجيه الشحنة الموجبة في الجزيء نحو الشحنة السالبة للجزيء الآخر ، وبما أن الجزيئات دائمًا في حركة ثابتة وتصادمات مستمرة مع بعضها البعض ، فإن هذا الوصف للجزيء عملية الجذب أبعد ما تكون عن الكمال ، خاصة في الغازات والسوائل ، ومع ذلك ، فإن التجاذب بين الأقطاب ذات الشحنات المعاكسة للجزيئات الثنائية يكون أكثر احتمالا من التجاذب بين الأقطاب المتنافرة بين أقطاب من نفس الشحنة ، وبالتالي فإن صافي الجذب الكلي هو شكلت.
مقارنة بين قوى التشتت وقوى ثنائية القطب
إذا نظرنا إلى مواضع جزيئات ثنائي القطب في الحالة السائلة والصلبة ، نجد ما يلي:
في الحالة الصلبة ، يحدث الجذب إذا كانت قوى الجذب كبيرة جدًا.
في الحالة السائلة: بسبب قدرة الجزيئات في الحالة السائلة على التحرك بشكل مستمر ، إذا حدث ذلك ، يجب أن تتخذ الأقطاب أوضاعًا معينة ، حيث تتخذ أوضاعًا جذابة مرة واحدة ومواقف مثيرة للاشمئزاز مرة أخرى.
في النهاية وجد أن نسبة التجاذب بين القطبين أعلى من التنافر بينهما، ووجد أن هذا يتناسب طرديًا مع مربع العزم القطبي، وعكسًا مع القوة السادسة للمسافة الفاصلة مركزي القطبين.